16.2: ciclos de vida Víricos
a via Lisogénica
uma melhor opção para alguns vírus bacterianos é chamada de Via lisogénica. Os bacteriófagos que têm esta opção, bem como uma via lítica, são conhecidos como fagos temperados. Nesta via, o vírus entra em dormência integrando-se no genoma do hospedeiro e permanecendo transcritivamente quiescente até que as condições ambientais se alterem e reflictam a probabilidade de mais células hospedeiras infectarem (figura \(\PageIndex{4}\)).
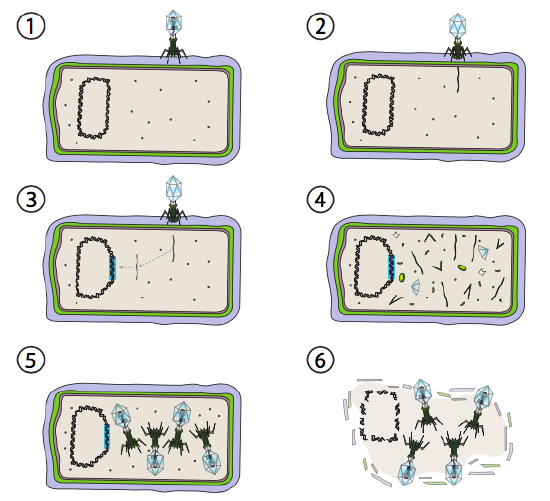
Lambda (λ) é um exemplo de bacteriofagem temperada. As fases iniciais da infecção e da injeção do genoma são as mesmas que o ciclo lítico, mas sob condições que incentivam a lisogenia, o genoma viral é integrado no genoma do hospedeiro na Etapa 3. Em uma integração em E. coli, isto ocorre por recombinação recíproca numa sequência de pares de 15 bases conhecida como local att λ e é facilitado pelo produto do gene Int. Enquanto as condições ambientais não conduzirem à reprodução bacteriana (e, portanto, um número limitado de células hospedeiras possíveis), o genoma viral permanece, na sua maioria, oculto e inactivo. A única exceção significativa é um gene que codifica um compressor λ Que impede o próximo passo e mantém o vírus dormente.
esse passo seguinte é a excisão do DNA fagoso λ do cromossomo hospedeiro, e subsequente replicação e transcrição do DNA viral (figura \(\PageIndex{4}\), Passo 4). Então, como antes, os passos finais são a montagem e acumulação de viriões, e eventual colapso da estrutura celular e libertação das partículas virais.
a fim de embalar dentro das restrições de espaço apertado oferecidas pelos capsídeos, os genomas virais devem ser altamente econômicos. Por exemplo, o genoma do HIV (figura \(\PageIndex{6}\)) tem vários genes que se sobrepõem.
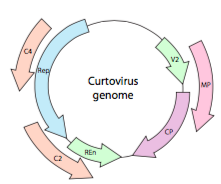
Ou, no caso de curtoviruses, ssDNA vírus em plantas (e.g. beterraba curly top de vírus), o genoma não só tem um Representante de lapidação de genes, é mesmo bi-direcional (Figura \(\PageIndex{7}\)) codificação de produtos de gene em ambos os filamentos de DNA após o ssDNA foi convertido para dsDNA.
dada a necessidade de economia, que genes são encontrados nos vírus? Um dos mais estudados genomas virais, de um bacteriófago λ, contém genes de codificação de cinco transcrição de controle de proteínas (que são expressas depende se o fago em um lysogenic ou líticas modo), uma proteína de ligação que controla a degradação de um ativador transcricional, 17 de proteínas da cápside, um excisionase que controla a excisão e a inserção do genoma do fago no host genoma, uma integração de proteína que insere o genoma do fago para o anfitrião, e 3 genes que participam na lise da célula hospedeira.
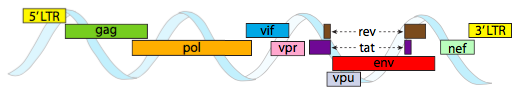
o genoma do HIV descrito acima é muito menor que λ, em torno de 9 quilobases em comparação com 48 kb, mas novamente, o tema é usar proteínas celulares quando possível, e codificar genes virais se necessário. Assim, gag codifica proteínas da cápside, pol codifica a transcriptase reversa, integrase e protease do HIV (que cliva o gag e pol produtos de gene em suas proteínas funcionais), vif atos contra comum célula hospedeira antiviral enzima, a vpr regula nuclear de importação, tat aumenta a transcrição de genes do HIV, rev exportações do RNA viral a partir do núcleo, vpu é necessária para brotação das partículas do host, env codifica as glicoproteínas do envelope viral, e nef promove a sobrevivência de células infectadas. As regiões do LTR são promotores muito fortes para impulsionar a alta expressão destes genes.
embora não seja referido como lisogenia, alguns vírus animais podem se comportar da mesma forma. O exemplo mais proeminente é o vírus Classe VI de Baltimore-comumente conhecido como retrovírus, um dos quais é HIV. O caminho de um retrovírus através de uma célula hospedeira eucariótica é descrito abaixo ( g. 5).
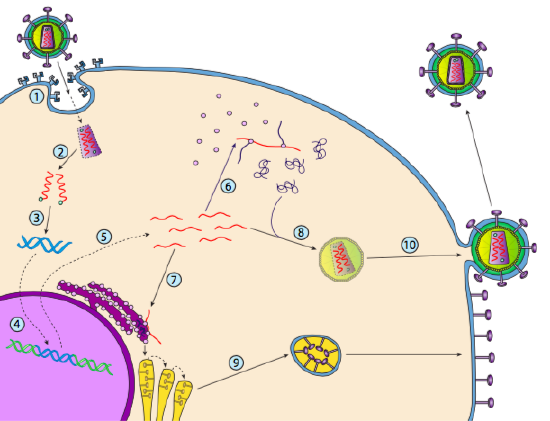
HIV tem um envelope, que é cravado com proteínas transmembranares que são reconhecidas pela célula hospedeira, ligando o vírus à superfície celular e iniciando endocitose mediada pelo receptor (1). Após a endocitose, o invólucro de membrana do virião e da membrana vesicular fundem-se para libertar o capsídeo e o seu conteúdo (2). Após a dissociação da capsida no citoplasma, as duas cadeias de RNA viral são liberadas juntamente com uma polimerase especial: transcriptase reversa, que lê um modelo de RNA e sintetiza DNA. A transcriptase reversa também usa esse novo DNA para sintetizar uma cadeia complementar de DNA de modo que ele eventualmente produz uma versão de DNA de cadeia dupla do genoma viral (3). Este dsDNA viral é transportado para o núcleo onde se integra no genoma do hospedeiro usando outra proteína viral, integrase
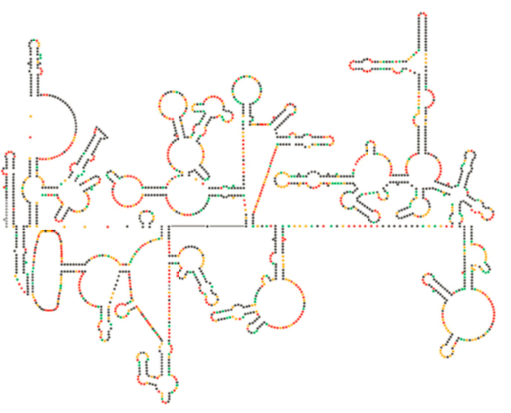
(4). O DNA viral integrado é chamado de provírus. O vírus pode ficar dormente, mas se é ativado, então é transcrito e o RNA viral resultante é transportado para fora do núcleo (5). Alguns de RNA viral codifica enzimas como transcriptase reversa e integrase, ou proteínas da cápside, que são feitos no citoplasma (6), mas alguns codificar membrana acoplado glicoproteínas, que são translocados para o ER (7) e, eventualmente, processados através de Golgi e incorporados na membrana plasmática (9). Uma vez que o virião foi montado (8), liga-se às proteínas transmembranares virais, nucleando uma “vesícula” exocítica (10) que é o virião completo com envelope viral.o recente exame estrutural do genoma do VIH sugere que a estrutura do próprio ARN do VIH pode desempenhar um papel significativo na sua propagação no interior das células hospedeiras. A figura \(\PageIndex{8}\), de Watts et al, Nature 460:711-716, 2009, mostra uma estrutura secundária prevista do genoma. Os autores sugerem que a estrutura de RNA realmente pode interagir com o alongamento ribossômico para controlar a dobragem das proteínas virais. Eles também postulam a extensão deste argumento para incluir informações genéticas importantes codificadas não apenas na sequência nucleotídica, mas na estrutura secundária e estrutura terciária de qualquer vírus RNA.
ao considerar os vírus em relação ao resto deste capítulo integrativo, há duas ideias fundamentais a ter em mente. Em primeiro lugar, a sobrevivência viral é baseada em números: precisa fazer um grande número de seus componentes para lançar uma rede o mais ampla possível para novas células hospedeiras. Para fazer isso, os promotores virais são geralmente muito mais fortes do que os promotores de células hospedeiras, simultaneamente conduzindo mais expressão do gene viral, ao mesmo tempo impedindo a expressão do gene hospedeiro (dedicando recursos celulares à produção de vírus). Em segundo lugar, devido aos tempos de geração rápida, a taxa de mutação viral e evolução é muito mais rápida do que os genomas eucarióticos normais. Além disso, se o vírus usa sua própria polimerase (como transcriptase reversa ou replicase RNA), a taxa de mutação aumenta ainda mais porque não há verificação de erros por polimerases virais.